Dãy hoạt động hóa học của kim loại gồm dãy các kim loại được sắp xếp theo thứ tự, thứ tự này phụ thuộc vào mức độ hoạt động của kim loại (tức là khả năng tham gia phản ứng hóa học với chất khác). Dãy hoạt động hóa học của kim loại được xây dựng từ phương pháp thực nghiệm.
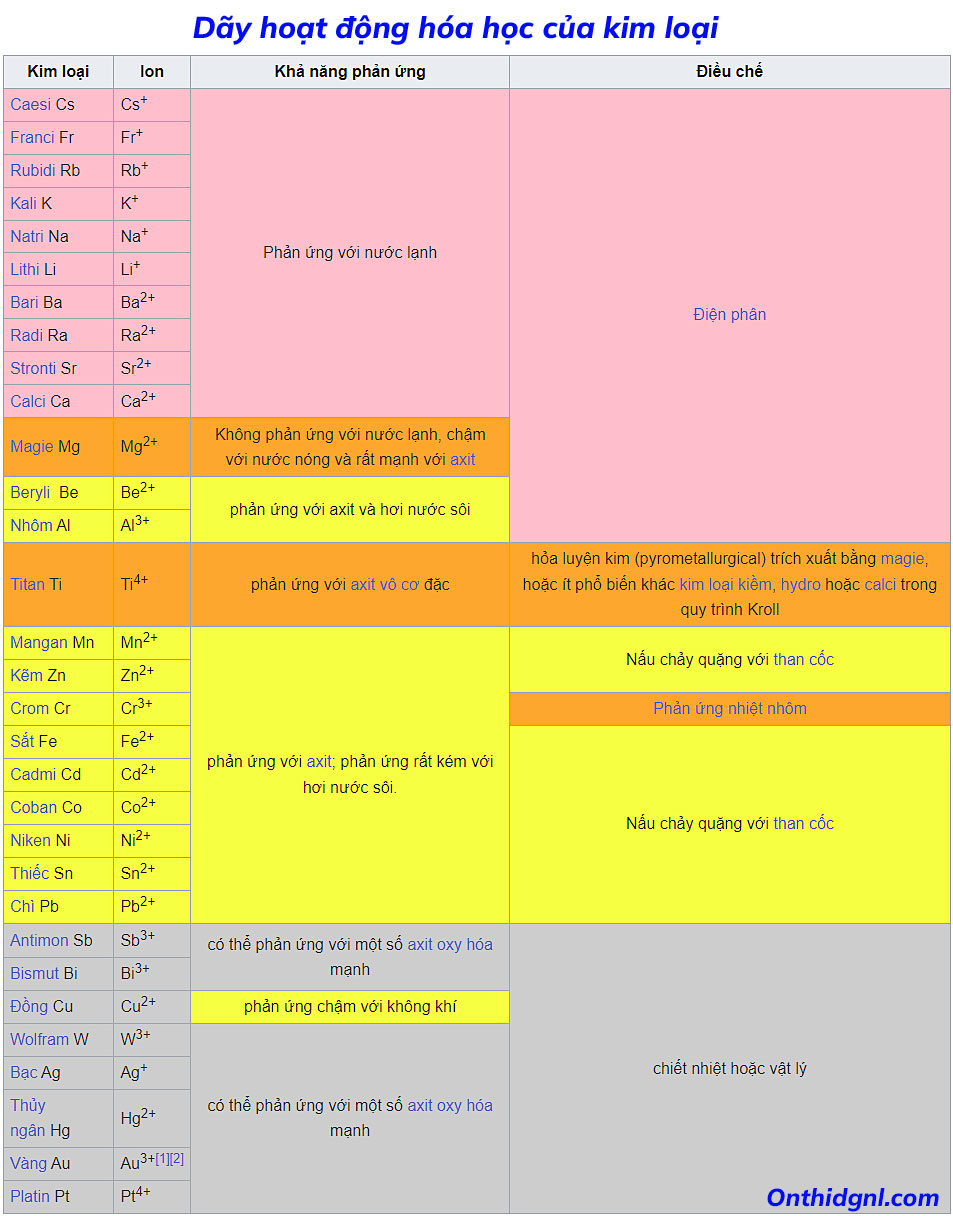
- Dãy hoạt động hóa học của kim loại là gì?
- Tính chất dãy hoạt động hóa học của kim loại
- Mức độ hoạt động giảm dần từ trái sang phải
- Các kim loại đứng trước Mg phản ứng với nước ở nhiệt độ thường
- Kim loại đứng trước H tác dụng với dung dịch axit tạo ra H2
- Kim loại không tan trong nước (từ Mg trở về sau) đẩy được kim loại đứng sau nó ra khỏi dung dịch muối
- Kim loại tác dụng với muối
- Cách ghi nhớ dãy hoạt động hóa học của kim loại
- Câu hỏi dãy điện hóa của kim loại
Dãy hoạt động hóa học của kim loại là gì?
Sau đây là dãy hoạt động hóa học của kim loại:
K, Ba, Ca, Na, Mg, Al, Zn, Cr, Fe, Ni, Sn, Pb, (H), Cu, Hg, Ag, Pt, Au
- Khi các kim loại được sắp xếp theo chiều giảm dần mức độ hoạt động hóa học của chúng thì được gọi là dãy hoạt động hóa học của kim loại.
- Một số kim loại sẽ có dãy hoạt động hóa học như sau:
Sau đây là một số tính chất hóa học của các chất trong kim loại
Kim loại tác dụng với
- Trong nhiệt độ thường: Ba, Na, Mg, Ca, K
- Trong nhiệt độ cao: Al, Zn, Fe, Ni, Sn, Pb, (H), Ag, Cu, An, Mg
- Khó có thể xảy ra phản ứng: Hg, Pt, Au
Kim loại tác dụng với nước:
- Kim loại có thể tác dụng với nước: K, Ba, Ca, Na, Mg
- Ở nhiệt độ thường không có phản ứng với nước: Al, Zn, Fe, Ni, Sn, Pb, (H), Cu, Ag, Hg, Pt, Au
Kim loại có phản ứng với axit thông thường:
- Giải phóng ra hidro khi tác dụng với axit thông thường: K, Ba, Ca, Na, Mg, Al, Zn, Fe, Ni, Sn, Pb, (H)
- Không có phản ứng: Cu, Ag, Hg, Pt, Au
Có tính khử oxit:
- Không khử được oxit bằng H2, CO: Ba, Ca, Na, Mg, Al, Zn
- Ở nhiệt độ cao khử được oxit kim loại này: Fe, Ni, Sn, Pb, (H), Cu, Hg, Ag, Pt
- Kim loại đứng sau bị đẩy ra khỏi muối bởi kim loại đứng trước: Al, Zn, Fe, Ni, Sn, Pb, (H), Cu, Ag, Hg, Pt, Au.
Tính chất dãy hoạt động hóa học của kim loại
Sau đây là tổng hợp các tính chất hóa học của kim loại cần lưu ý
Mức độ hoạt động giảm dần từ trái sang phải
- Au sẽ là kim loại hoạt động kém nhất còn K là kim loại hoạt động mạnh nhất
- Nhóm các kim loại mạnh nhất gồm có: Li, K, Ba, Ca, Na
- Các ki: Mg, Al
- Nhóm các kim loại trung bình gồm có: Mn, Zn, Cr, Fe, Ni, Sn, Pb
- Các kim loại yếu gồm: Hg Pt, Au, Cu, Ag
Các kim loại đứng trước Mg phản ứng với nước ở nhiệt độ thường
Kim loại phản ứng với nước ở nhiệt độ thường là K, Ba, Ca, Na
Các kim loại không tác dụng với nước ở nhiệt độ thường là Al, Zn, Fe, Ni, Sn, Pb, (H), Cu, Ag, Hg, Pt, Au
Các kim loại phản ứng với nước ở nhiệt độ thường là những kim loại đứng trước Mg, bao gồm: K, Ba, Ca, Các phương trình của phản ứng này như sau:
2Na + 2H2O → 2NaOH + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
Kim loại đứng trước H tác dụng với dung dịch axit tạo ra H2
Các kim loại đứng trước H khi tác dụng với dung dịch axit ví dụ như HCl, H2SO4 loãng,… sẽ tạo ra H2
Các kim loại có phản ứng là: K, Ba, Ca, Na, Mg, Al, Zn, Fe, Ni, Sn, Pb, (H)
Các kim loại không có phản ứng là: Cu, Ag, Hg, Pt, Au
Để xảy ra phản ứng phải thỏa mãn hai điều kiện
- Nguyên tố hidro trong dãy hoạt động hóa học đứng sau kim loại đó
- Axit loãng là dung dịch kim loại phản ứng
Fe + 2HCl → FeCl2 + H2 ↑
Cu + 2HCl → không phản ứng (H đứng trước Cu)
Kim loại không tan trong nước (từ Mg trở về sau) đẩy được kim loại đứng sau nó ra khỏi dung dịch muối
Các phương trình hóa học của phản ứng này là:
Fe + CuSO4 → FeSO4 + Cu
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Kim loại tác dụng với muối
- Kim loại của hợp chất phải đứng sau kim loại của đơn chất (trong dãy hoạt động hóa học)
- Từ Mg trở về sau là kim loại của đơn chất (là Mg, Al, Zn,…)
Ví dụ: Muối của Fe và Zn phản ứng với nhau sẽ có phương trình:
Mg + FeCl2 → MgCl2 + Fe
Cách ghi nhớ dãy hoạt động hóa học của kim loại
Để nhớ nhanh được bảng kim loại hơn, thì sau đây là hai cách nhớ mẹo mà các em học sinh có thể ghi nhớ để áp dụng khi làm bài:
* Mẹo nhớ như sau
Khi (K) bà (Ba) con (Ca) nào (Na) may (Mg) áo (Al) giáp (Zn) sắt (Fe) nhớ (Ni) sang (Sn) phố (Pb) hỏi (H) cửa (Cu) hàng (Hg) á (Ag) phi (Pt) âu (Au)
Hoặc:
Khi (K) cần (Ca) nàng (Na) may (Mg) áo (Al) giáp (Zn) sắt (Fe) nhớ (Ni) sang (Sn) phố (Pb) hỏi (H) cửa (Cu) hàng (Hg) Á (Ag) Phi (Pt) Âu (Au)
Câu hỏi dãy điện hóa của kim loại
Câu1: Chiều hoạt động hóa học giảm dần là tính chất của dãy kim loại nào dưới đây
- A. Na, Mg, Zn
- B, Al, Zn, Na
- C, Mg, Al, Na
- D, Pb, Al, Mg
Câu 2: Zn(NO3)2 lẫn Cu(NO3)2 và AgNO3 được làm sạch bởi kim loại nào dưới đây
- A, Zn
- B, Cu
- C, Fe
- D, Pb
Câu 3: Dung dịch HCl dư được cho 4,8 gam kim loại M có hóa trị II vào, từ đó thoát ra 4,48 lít khí hidro (ở đktc). Kim loại đó là gì
- A, Ca
- B, Mg
- C, Fe
- D, Ba
Câu 4: Mg trong dãy hoạt động hóa học có 4 kim loại đứng sau là X, Y, Z, T đứng sau. Trong dung dịch HCl, biết Z và T tan. Trong dung dịch HCl, X và Y không tan , trong dung dịch muối T, Z đẩy được T. Trong dung dịch muối Y, X đẩy được Y. Đâu là dãy hoạt động hóa học tăng dần
- A, T, Z, X, Y
- B, Z, T, X, Y
- C, Y, X, T, Z
- D, Z, T, Y, X
Câu 5: Thể tích khí thoát ra (ở đktc) khi cho 5,4 gam nhôm vào dung dịch HCl dư
- A. 4,48 l
- B. 6,72 l
- C, 13,44 l
- D, 8,96 l
Câu 6: Cân lại lá đồng sau khi cho vào AgNO3 một thời gian, khối lượng lá đồng sẽ thế nào
- A, Tăng
- B, Giảm
- C, Không tăng, không giảm
- D, Giảm một nửa
Câu 7: Hiện tượng xảy ra khi cho 1 viên Natri phản ứng với CuSO4
- A, Dung dịch không đổi màu, sủi bọt khí, viên Natri tan dần
- B, Không có khí thoát ra, có kết tủa màu xanh lam, viên Natri tan dần
- C, Có khí không màu thoát ra, xuất hiện kết tủa màu xanh lam, viên Natri tan,
- D, Không xảy ra phản ứng gì.
Câu 8: Dung dịch H2SO4 hoà tan 32,5 gam kim loại (hoá trị II) loãng được 11,2 lít khí hiđro (ở đktc). Kim loại đó là
- A, Zn
- B, Fe
- C, Mg
- D, Cu
Câu 9: Trong dung dịch CuSO4 có 1 lá Zn được ngâm, sau 1 thời gian khối lượng dung dịch tăng 0,2g khi lấy là Zn ra. Zn có khối lượng phản ứng là
- A, 0,2 g
- B, 13 g
- C, 6,5 g
- D, 0,4 g
Câu 10: Al và Cu là 10g hỗn hợp được đưa vào dung dịch HCl dư, đưa ra 6,72l khí hidro (đktc). Nhôm có bao nhiêu phần trăm trong hỗn hợp?
- A, 81 %
- B, 54 %
- C, 27 %
- D, 40 %
| 1. A | 2. A | 3. B | 4. C | 5. B |
| 6. A | 7. C | 8. A | 9. B | 10. B |
Có thể nói, Dãy hoạt động hóa học của kim loại là phần rất quan trọng trong kiến thức chất vô cơ, để học tốt hóa học 12 buộc các bạn phải nắm rõ và hiểu lý thuyết; tổng hợp được kiến thức hóa học THPT để thi tốt nghiệp hoặc ôn thi đánh giá năng lực hiệu quả.
Theo dõi MXH của Onthidgnl để update nhiều tài liệu miễn phí nhé:
FB: https://www.facebook.com/onthidgnlcom
